PQQ. Générer des mitochondries fraîches avec PQQ
Les scientifiques découvrent le “Autre CoQ10”
 En 1983, Life Extension® a introduit un composé relativement peu connu appelé coenzyme Q10. Notre revue de la littérature à l'époque avait mis au jour des données confirmant son pouvoir d'améliorer la santé et la production d'énergie des mitochondries.
En 1983, Life Extension® a introduit un composé relativement peu connu appelé coenzyme Q10. Notre revue de la littérature à l'époque avait mis au jour des données confirmant son pouvoir d'améliorer la santé et la production d'énergie des mitochondries.
Les scientifiques reconnaissent aujourd'hui que le dysfonctionnement mitochondrial est un biomarqueur clé du vieillissement.1-6 Pour prendre un exemple, les chercheurs ont enregistré des preuves de 50% plus de dommages mitochondriaux dans les cellules cérébrales d’êtres humains de plus de 70 ans par rapport aux individus d’âge moyen7. Le dysfonctionnement mitochondrial et la mort sont désormais définitivement liés au développement de pratiquement toutes les maladies mortelles du vieillissement, de l’Alzheimer et du diabète de type 2 à l’insuffisance cardiaque.8-11
La bonne nouvelle est que le dysfonctionnement mitochondrial peut être inversé12. La littérature scientifique regorge d’études documentant le pouvoir thérapeutique de la CoQ10 pour lutter contre les maladies dégénératives en améliorant la santé mitochondriale et la capacité bioénergétique (production d’énergie) 13-16.
La dernière avancée dans le domaine de la bioénergétique mitochondriale est la coenzyme pyrroloquinoléine quinone ou PQQ.
Le rôle critique du PQQ dans diverses fonctions biologiques n’est apparu que progressivement. Comme la CoQ10, il s’agit d’un micronutriment dont la capacité antioxydante constitue un moyen de défense extraordinaire contre la pourriture mitochondriale.
Mais la révélation la plus intéressante sur le PQQ est apparue au début de 2010, lorsque les chercheurs ont découvert qu'elle protégeait non seulement les mitochondries des dommages oxydatifs, mais stimulait également la croissance de nouvelles mitochondries! 17
Dans cet article, vous découvrirez la capacité de ce nouveau coenzyme à lutter contre le dysfonctionnement mitochondrial. Vous découvrirez comment il protège le cerveau, le cœur et les muscles contre les maladies dégénératives. Vous découvrirez également son potentiel pour inverser le vieillissement cellulaire en activant les gènes qui induisent la biogenèse mitochondriale - la formation spontanée de nouvelles mitochondries dans les cellules vieillissantes!
PQQ: Une percée dans l'anti-vieillissement cellulaire
 PQQ est omniprésent dans le monde naturel. Sa présence dans les poussières d'étoiles interstellaires a conduit certains experts à émettre l'hypothèse d'un rôle déterminant pour le PQQ dans l'évolution de la vie sur Terre.18Il a été trouvé chez toutes les espèces de plantes testées à ce jour. Ni les humains ni les bactéries qui colonisent le tube digestif humain n'ont démontré la capacité de le synthétiser.19 Cela a conduit les chercheurs à classer le PQQ parmi les micronutriments essentiels .20
PQQ est omniprésent dans le monde naturel. Sa présence dans les poussières d'étoiles interstellaires a conduit certains experts à émettre l'hypothèse d'un rôle déterminant pour le PQQ dans l'évolution de la vie sur Terre.18Il a été trouvé chez toutes les espèces de plantes testées à ce jour. Ni les humains ni les bactéries qui colonisent le tube digestif humain n'ont démontré la capacité de le synthétiser.19 Cela a conduit les chercheurs à classer le PQQ parmi les micronutriments essentiels .20
Le potentiel de PQQ pour stimuler la biogenèse mitochondriale a été prédit par de nombreuses découvertes préliminaires indiquant son rôle central dans la croissance et le développement de multiples formes de vie.
Il a été démontré qu’il était un facteur de croissance puissant chez les plantes, les bactéries et les organismes supérieurs 21,22. Des études précliniques révèlent que, lorsqu'ils sont privés de PQQ alimentaire, les animaux présentent un retard de croissance, une immunité compromise, une capacité de reproduction altérée et, plus important encore, une diminution du nombre de mitochondries dans leurs tissus. Les taux de conception, le nombre d'enfants et les taux de survie chez les animaux juvéniles sont également considérablement réduits en l'absence de PQQ.23-25 Le fait de réintroduire la PQQ dans le régime inverse ces effets, en restaurant la fonction systémique tout en augmentant simultanément le nombre de mitochondries et l'efficacité énergétique.
Défense mitochondriale optimale
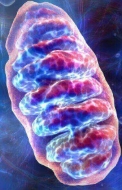 Principaux moteurs de la quasi-totalité de la production de bioénergie, les mitochondries font partie des structures physiologiques les plus vulnérables à la destruction par dommage oxydatif. La formidable capacité de piégeage des radicaux libres de PQQ confère aux mitochondries une protection antioxydante supérieure.
Principaux moteurs de la quasi-totalité de la production de bioénergie, les mitochondries font partie des structures physiologiques les plus vulnérables à la destruction par dommage oxydatif. La formidable capacité de piégeage des radicaux libres de PQQ confère aux mitochondries une protection antioxydante supérieure.
Une stabilité moléculaire extraordinaire est au cœur de cette capacité.30 En tant que coenzyme bioactive, PQQ participe activement au transfert d'énergie au sein de la mitochondrie qui fournit au corps l'essentiel de sa bioénergie (comme la CoQ10).
Contrairement aux autres composés antioxydants, la stabilité exceptionnelle du PQQ lui permet d’effectuer des milliers de transferts d’électrons sans subir de dégradation moléculaire. Il s'est avéré particulièrement efficace pour neutraliser les radicaux superoxydes et hydroxyles 31.
Selon les recherches les plus récentes, «le PQQ est 30 à 5 000 fois plus efficace pour maintenir le cycle redox (production d'énergie mitochondriale). . . que d'autres [composés antioxydants] courants, par ex. acide ascorbique. ”21 Une découverte constante dans la littérature scientifique est que les nutriments comme le PQQ offrent des avantages plus variés que les antioxydants classiques sur lesquels le grand public compte.
Armure anti-âge pour les organes les plus énergivores
La double capacité de PQQ en tant que modulateur de signalisation cellulaire et antioxydant supérieur le rend efficace dans la lutte contre les maladies dégénératives et le déclin lié à l’âge des organes les plus énergétiques du corps: le cœur et le cerveau.
La révélation de sa capacité à influencer favorablement le développement cellulaire, le métabolisme et la biogénèse mitochondriale à l’échelle du système fournit une explication à une profusion de données sur ses avantages neuroprotecteurs et cardioprotecteurs.
Neuroprotection
 Il a été démontré que PQQ optimisait la santé et le fonctionnement de tout le système nerveux central. Il inverse les déficiences cognitives causées par le stress oxydatif chronique dans les modèles précliniques, améliorant ainsi les performances des tests de mémoire32. Il a également été démontré qu'il protégeait le «gène de la maladie de Parkinson», DJ-1, de l'auto-oxydation - une étape précoce dans l'apparition de la maladie33.
Il a été démontré que PQQ optimisait la santé et le fonctionnement de tout le système nerveux central. Il inverse les déficiences cognitives causées par le stress oxydatif chronique dans les modèles précliniques, améliorant ainsi les performances des tests de mémoire32. Il a également été démontré qu'il protégeait le «gène de la maladie de Parkinson», DJ-1, de l'auto-oxydation - une étape précoce dans l'apparition de la maladie33.
Les espèces réactives à l'azote (RNS), comme les espèces réactives à l'oxygène, imposent des contraintes sévères aux neurones endommagés34. Ils surviennent spontanément à la suite d'un accident vasculaire cérébral et de lésions de la moelle épinière et il a été démontré qu'une part importante des lésions neurologiques ultérieures à long terme était importante. La PQQ supprime le RNS lors d’AVC induits expérimentalement .35 Il fournit également une protection supplémentaire en bloquant l'expression génique de l'oxyde nitrique synthase (iNOS) inductible, une source majeure de RNS, à la suite d'une lésion de la moelle épinière36.
Le PQQ protège puissamment les cellules du cerveau contre les dommages oxydatifs consécutifs aux lésions d'ischémie-reperfusion, à savoir les dommages inflammatoires et oxydatifs résultant du retour soudain de sang et de nutriments dans des tissus qui en étaient privés par accident vasculaire cérébral37. Administré immédiatement avant l'induction d'un accident vasculaire cérébral chez des modèles animaux, le PQQ réduit considérablement la taille de la zone cérébrale endommagée38.
Le PQQ interagit également de manière bénéfique avec les systèmes de neurotransmetteurs de notre cerveau. En particulier, PQQ protège les neurones en modifiant l’important site du récepteur NMDA.39,40 Le NMDA est un puissant médiateur de «l'excitotoxicité», une réponse à la surstimulation à long terme des neurones associée à de nombreuses maladies neurodégénératives et crises épileptiques. 41-43 Le PQQ protège également contre la neurotoxicité induite par d'autres toxines, y compris le mercure44,45.
De plus en plus de preuves suggèrent que la QPQ constitue une intervention puissante dans la maladie d’Alzheimer et la maladie de Parkinson. Les deux sont déclenchés par l'accumulation de protéines anormales qui initient une cascade d'événements oxydatifs entraînant la mort des cellules cérébrales. La PQQ empêche le développement d’une protéine (alpha-synucléine) associée à la maladie de Parkinson46. Il protège également les cellules nerveuses des ravages oxydants de la protéine bêta-amyloïde liée à la maladie d’Alzheimer.47 Une étude de 2010 a révélé que le PQQ pourrait empêcher la formation de structures moléculaires bêta-amyloïdes48.
Il a également été démontré que le PQQ protège la mémoire et la cognition chez les animaux et les humains vieillissants.49,50Il stimule la production et la libération du facteur de croissance nerveuse dans les cellules qui supportent les neurones dans le cerveau51. Cela peut expliquer en partie pourquoi la supplémentation en PQQ de rats âgés a entraîné une nette amélioration de leur fonction de mémoire49.
Chez l'homme, une supplémentation de 20 mg par jour de PQQ a permis d'améliorer les tests de la fonction cognitive supérieure dans un groupe de personnes d'âge moyen et âgées50. Ces effets ont été amplifiés de manière significative lorsque les sujets ont également pris 300 mg de CoQ10 par jour.
 La dysfonction mitochondriale a été définitivement liée à pratiquement toutes les maladies mortelles du vieillissement, de la maladie d’Alzheimer au diabète de type 2 en passant par l’insuffisance cardiaque.
La dysfonction mitochondriale a été définitivement liée à pratiquement toutes les maladies mortelles du vieillissement, de la maladie d’Alzheimer au diabète de type 2 en passant par l’insuffisance cardiaque.- Les chercheurs ont enregistré des preuves de lésions mitochondriales plus importantes dans les cellules cérébrales des personnes de plus de 70 ans par rapport à celles du début de la quarantaine.
- De nombreux scientifiques pensent que la longévité des mitochondries détermine la longévité globale.
- Une coenzyme de nouvelle génération, appelée pyrroloquinoléine quinone ou PQQ, est en train d'introduire une biogénèse mitochondriale, la croissance de nouvelles mitochondries dans les cellules vieillissantes.
- Alors que la CoQ10 optimise la fonction mitochondriale, la PQQ active les gènes qui régissent la reproduction, la protection et la réparation mitochondriales.
- Le PQQ offre également une cardioprotection et une défense puissantes contre la dégénérescence neuronale (cerveau).
- Des études publiées montrent que 20 mg de PQQ plus 300 mg de CoQ10 pourraient inverser le déclin cognitif lié à l'âge chez les humains vieillissants.
Fonction mitochondriale et longévité: Le lien définitif
 En biologie cellulaire, les mitochondries sont uniques parmi les autres composants cellulaires dans un aspect vital: elles possèdent leur propre ADN primitif, distinct de l'ADN hébergé dans le noyau cellulaire que vous considérez normalement comme le bloc constitutif de tous les organismes vivants.
En biologie cellulaire, les mitochondries sont uniques parmi les autres composants cellulaires dans un aspect vital: elles possèdent leur propre ADN primitif, distinct de l'ADN hébergé dans le noyau cellulaire que vous considérez normalement comme le bloc constitutif de tous les organismes vivants.
L’ADN mitochondrial ressemble beaucoup à l’ADN bactérien, résultat d’un héritage évolutif.55 Les biologistes pensent qu’à un moment donné, nos mitochondries existaient en tant qu’organismes distincts très énergétiques. Nos cellules ancestrales primordiales ont englouti et incorporé de manière agressive ces «proto-mitochondries» dans leur propre structure interne. Cela a procuré à nos géniteurs cellulaires deux avantages évolutifs puissants: il a mis à profit la capacité des proto-mitochondries à produire de grandes quantités d’énergie à partir de l’oxygène et a permis de renforcer la longévité cellulaire.
Ce simple fait a de profondes implications pour la science de l'anti-vieillissement.
Pourquoi? Vous savez déjà que les cellules de votre corps ont la capacité de se diviser et de se répliquer en raison de la présence d'ADN nucléaire. Si les mitochondries possèdent leur propre ADN, elles devraient également avoir la capacité de se répliquer et d’augmenter leur nombre au sein d’une seule cellule humaine.
Cela s'avère être le cas: les cellules humaines peuvent contenir de 2 à 2 500 mitochondries, 56, 58, selon le type de tissu, la nutrition, le statut antioxydant et d'autres facteurs. En d'autres termes, une cellule peut contenir plus de 1 000 fois plus de mitochondries qu'un autre.
Plus les mitochondries de votre corps sont performantes, plus votre santé et votre longévité seront grandes. Ce n'est plus une question de conjecture. Un nombre croissant de biologistes cellulaires adhèrent maintenant à la théorie selon laquelle le nombre et la fonction des mitochondries déterminent la longévité humaine.59-61
Le problème est que les méthodes scientifiquement validées disponibles pour augmenter spontanément le nombre de nouvelles mitochondries dans nos corps vieillissants sont extrêmement difficiles. À ce jour, les seuls moyens connus de stimuler de manière fiable la biogenèse mitochondriale - restriction durable des calories ou activité physique intense - sont beaucoup trop rigoureux et peu pratiques pour la plupart des individus vieillissants.
Un nutriment capable de déclencher en toute sécurité la biogenèse mitochondriale marquerait naturellement une avancée extraordinaire dans la quête pour arrêter et inverser le vieillissement cellulaire.
Le PQQ est devenu ce nutriment.
Cardioprotection
Comme pour les accidents vasculaires cérébraux, les lésions cardiaques sont causées par des lésions d'ischémie-reperfusion. La supplémentation en PQQ réduit la taille des zones endommagées dans les modèles animaux de crise cardiaque aiguë (infarctus du myocarde).52Cela se produit que le supplément soit donné avant ou après l'événement ischémique lui-même.
Afin d'étudier plus avant ce potentiel, des chercheurs du VA Medical Center de l'UC-San Francisco ont comparé le PQQ au métoprolol, un bêta-bloquant qui est un traitement clinique standard post-IM. Seuls les deux traitements ont permis de réduire la taille des zones endommagées et de les protéger contre le dysfonctionnement du muscle cardiaque. Quand ils ont été administrés ensemble, la pression de pompage du ventricule gauche a été augmentée. La combinaison augmentait également les fonctions de production d'énergie mitochondriale - mais l'effet était faible comparé au PQQ seul! Et seul le PQQ a favorablement réduit la peroxydation lipidique. La conclusion remarquable: «Le PQQ est supérieur au métoprolol en ce qu'il protège les mitochondries des dommages oxydatifs dus à l'ischémie / reperfusion.» 53
Des recherches ultérieures de la même équipe ont démontré que le PQQ aide les cellules du muscle cardiaque à résister au stress oxydatif aigu54.
Le mécanisme? Préserver et améliorer la fonction mitochondriale.
Pourquoi vos mitochondries sont fortement exposées à la mutation létale
 Le vieillissement cellulaire se produit lorsque la capacité de chaque cellule à se reproduire diminue inexorablement. Ce déclin est à son tour associé à la dégradation et à la destruction graduelles du complexe de l'ADN.
Le vieillissement cellulaire se produit lorsque la capacité de chaque cellule à se reproduire diminue inexorablement. Ce déclin est à son tour associé à la dégradation et à la destruction graduelles du complexe de l'ADN.
On oublie dans ce processus le rôle tout aussi important de la capacité robuste de la mitochondrie à se reproduire avec l'âge.
Tout comme la dégradation du complexe de l'ADN cellulaire conduit finalement à la sénescence et à la mort, la dégradation du complexe de l'ADN mitochondrial entraîne la mort de la mitochondrie et l'extinction ultime de la cellule - et de l'organisme «hôte».
Cette spirale de mort de dégradation génétique est accélérée dans les mitochondries par la fonction physiologique même qu'elles doivent remplir. Générateurs nucléaires responsables de la quasi-totalité de la production bioénergétique, les mitochondries sont le site d’une énorme activité oxydante. Un nombre presque incalculable d'électrons circulent constamment dans les mitochondries, rejetant un nombre non moins énorme de radicaux libres. Cela les rend très vulnérables aux insultes biochimiques.
Les scientifiques ont découvert au cours des dernières décennies qu'il existe une menace supplémentaire: par rapport à l'ADN nucléaire, l'ADN mitochondrial possède peu de moyens de défense contre les dommages des radicaux libres.62,63
L'ADN cellulaire est protégé par de nombreuses protéines «tutrices» (histones et enzymes de réparation) qui atténuent l'impact des radicaux libres. Aucun système de réparation de ce type n'existe pour protéger l'ADN mitochondrial.
L'ADN cellulaire bénéficie également de défenses structurelles supérieures. Il est logé dans une double membrane protectrice qui le sépare du reste de la cellule. Cette double membrane est complétée par une matrice dense de protéines filamenteuses appelée membrane nucléaire, une sorte de coque dure pour protéger davantage l'ADN des impacts externes.
À titre de comparaison, l’ADN mitochondrial est presque entièrement exposé: il se fixe directement à la membrane interne où le four électrochimique des mitochondries fonctionne en permanence, générant un volume énorme d’espèces réactives de l’oxygène réactif.
En conséquence, l’ADN mitochondrial subit une mutation beaucoup plus rapide que l’ADN cellulaire. Lorsque vous considérez que les mitochondries fournissent au moins 95% de l'énergie nécessaire à tous les processus physiologiques de votre corps, la nécessité de maintenir l'intégrité de l'ADN mitochondrial revêt une urgence encore plus grande. Tous les êtres humains vieillissants doivent prendre toutes les mesures nécessaires pour protéger les gènes qui régulent la prolifération mitochondriale saine des mutations mortelles. Ceci est corroboré par l'abondance d'études scientifiques établissant un lien entre la mutation génétique au sein de la mitochondrie et le vieillissement humain65-67.
L’extraordinaire capacité antioxydante de PQQ représente une nouvelle intervention puissante qui peut renforcer efficacement les défenses limitées des mitochondries.
Une équipe de chercheurs de l’Université de Californie a décidé d’analyser l’influence du PQQ sur les voies de signalisation cellulaire impliquées dans la génération de nouvelles mitochondries17.
Leur travail, publié en 2010, a conduit à plusieurs découvertes extraordinaires.
Ils ont constaté que le rôle crucial du PQQ dans la croissance et le développement tenait à sa capacité unique à activer les voies de signalisation cellulaire directement impliquées dans le métabolisme, le développement et le fonctionnement de l’énergie cellulaire. Les cellules subissent une biogenèse mitochondriale spontanée sous l’effet de trois molécules de signalisation activées par la PQQ:
PQQ active l'expression de PCG-1α (coactivateur gamma 1-alpha activé par le récepteur activé par les proliférateurs de peroxysomes). PCG-1α est un «régulateur principal» qui mobilise la réponse de vos cellules à divers déclencheurs externes.Il stimule directement les gènes qui améliorent la respiration, la croissance et la reproduction cellulaires et mitochondriales. Sa capacité à réguler positivement le métabolisme cellulaire au niveau génétique a une incidence favorable sur la pression artérielle, la dégradation du cholestérol et des triglycérides et l'apparition de l'obésité26.
PQQ déclenche une protéine de signalisation appelée CREB (protéine de liaison aux éléments de réponse à l'AMPc). Le CREB joue un rôle central dans le développement et la croissance embryonnaires. Il interagit également de manière bénéfique avec les histones, des composés moléculaires qui protègent et réparent l'ADN cellulaire.27 Le CREB stimule également la croissance de nouvelles mitochondries.
PQQ régule une protéine de signalisation cellulaire récemment découverte appelée DJ-1. Comme avec PCG-1α et CREB, DJ-1 est intrinsèquement impliqué dans la fonction cellulaire et la survie. Il a été démontré que la prévention de la mort cellulaire par la lutte contre le stress antioxydant intense28,29 était particulièrement importante pour la santé et le fonctionnement du cerveau. Les dommages et les mutations de DJ-1 ont été liés de manière concluante à l’apparition de la maladie de Parkinson et d’autres troubles neurologiques.
Ces résultats mettent en lumière les résultats d'études antérieures selon lesquelles un déficit en PQQ chez des souris juvéniles, par exemple, entraînait des concentrations de glucose plasmatique élevées, une réduction de 20 à 30% du nombre de mitochondries dans le foie et, par conséquent, une altération du métabolisme de l'oxygène. 23 Ce sont des indicateurs caractéristiques du dysfonctionnement mitochondrial. D'autres modèles animaux ont également suggéré des modifications significatives du nombre de mitochondries. 25 Pris ensemble, ces résultats confirment le pouvoir de PQQ d’augmenter considérablement le nombre et la fonction des mitochondries, clé de l’anti-vieillissement cellulaire et de la longévité.
Résumé
La dysfonction mitochondriale a été définitivement liée à pratiquement toutes les maladies mortelles du vieillissement, de la maladie d’Alzheimer au diabète de type 2 en passant par l’insuffisance cardiaque.
Les chercheurs ont enregistré des preuves de lésions mitochondriales plus importantes dans les cellules cérébrales des personnes de plus de 70 ans par rapport à celles du début de la quarantaine. La santé et la fonction de ces générateurs d’énergie cellulaire sont à présent considérées comme si vitales que de nombreux scientifiques pensent que la longévité des mitochondries détermine la longévité globale chez les humains vieillissants.
Dans une avancée révolutionnaire, une coenzyme essentielle appelée pyrroloquinoléine quinone ou PQQ s'est avérée induire une biogenèse mitochondriale - la croissance de nouvelles mitochondries dans les cellules vieillissantes!
Alors que la CoQ10 optimise la fonction mitochondriale, la PQQ active les gènes qui régissent la reproduction, la protection et la réparation mitochondriales. La PQQ offre également une cardioprotection puissante et une défense optimale contre la dégénérescence neuronale. Des études publiées montrent que 20 mg de PQQ plus 300 mg de CoQ10 pourraient inverser le déclin cognitif lié à l'âge chez les humains vieillissants.
Matériel utilisé avec la permission de Life Extension. Tous les droits sont réservés.
- Bliznakov EG. Aging, mitochondria, and coenzyme Q(10): the neglected relationship. Biochimie. 1999 Dec;81(12):1131-2.
- Linnane AW, Marzuki S, Ozawa T, Tanaka M. Mitochondrial DNA mutations as an important contributor to ageing and degenerative diseases. Lancet. 1989 Mar 25;1(8639):642-5.
- Lanza IR, Nair KS. Mitochondrial metabolic function assessed in vivo and in vitro. Curr Opin Clin Nutr Metab Care. 2010 Sept;13(5):511.
- Mota MP, Peixoto FM, Soares JF, et al. Influence of aerobic fitness on age-related lymphocyte DNA damage in humans: relationship with mitochondria respiratory chain and hydrogen peroxide production. Age (Dordr). 2010 Sept;32(2):337-46.
- Tranah G. Mitochondrial-nuclear epistasis: Implications for human aging and longevity. Ageing Res Rev. 2010 Jun 25.
- Cho DH, Nakamura T, Lipton SA. Mitochondrial dynamics in cell death and neurodegeneration. Cell Mol Life Sci. 2010 Oct;67(20):3435-47.
- Mecocci P, MacGarvey U, Kaufman AE, et al. Oxidative damage to mitochondrial DNA shows marked age-dependent increases in human brain. Ann Neurol. 1993 Oct;34(4):609-16.
- Bugger H, Abel ED. Mitochondria in the diabetic heart. Cardiovasc Res. 2010 Jul 16.
- Conley KE, Amara CE, Jubrias SA, Marcinek DJ. Mitochondrial function, fibre types and ageing: new insights from human muscle in vivo. Exp Physiol. 2007 Mar;92(2):333-9.
- Lesnefsky EJ, Moghaddas S, Tandler B, Kerner J, Hoppel CL. Mitochondrial dysfunction in cardiac disease: ischemia—reperfusion, aging, and heart failure. J Mol Cell Cardiol. 2001 Jun;33(6):1065-89.
- Maruszak A, Zekanowski C. Mitochondrial dysfunction and Alzheimer’s disease. Prog Neuropsychopharmacol Biol Psychiatry. 2010 Jul 15.
- Conley KE, Marcinek DJ, Villarin J. Mitochondrial dysfunction and age. Curr Opin Clin Nutr Metab Care. Nov 2007;10(6):688-692.
- Bliznakov EG. Aging, mitochondria, and coenzyme Q(10): the neglected relationship. Biochimie. 1999 Dec;81(12):1131-2.
- Ochoa JJ, Quiles JL, Lopez-Frias M, Huertas JR, Mataix J. Effect of lifelong coenzyme Q10 supplementation on age-related oxidative stress and mitochondrial function in liver and skeletal muscle of rats fed on a polyunsaturated fatty acid (PUFA)-rich diet. J Gerontol A Biol Sci Med Sci. 2007 Nov;62(11):1211-8.
- Janson M. Orthomolecular medicine: the therapeutic use of dietary supplements for anti-aging. Clin Interv Aging. 2006;1(3):261-5.
- Linnane AW, Degli Esposti M, Generowicz M, Luff AR, Nagley P. The universality of bioenergetic disease and amelioration with redox therapy. Biochim Biophys Acta. 1995 May 24;1271(1):191-4.
- Chowanadisai W, Bauerly KA, Tchaparian E, Wong A, Cortopassi GA, Rucker RB. Pyrroloquinoline quinone stimulates mitochondrial biogenesis through cAMP response element-binding protein phosphorylation and increased PGC-1alpha expression. J Biol Chem. 2010 Jan 1;285(1):142-52.
- Rucker R, Chowanadisai W, Nakano M. Potential physiological importance of pyrroloquinoline quinone. Altern Med Rev. 2009 Sep;14(3):268-77.
- Smidt CR, Bean-Knudsen D, Kirsch DG, Rucker RB. Does the intestinal microflora synthesize pyrroloquinoline quinone? Biofactors.1991 Jan;3(1):53-9.
- Zhang Y, Rosenberg PA. The essential nutrient pyrroloquinoline quinone may act as a neuroprotectant by suppressing peroxynitrite formation. Eur J Neurosci. 2002 Sep;16(6):1015-24.
- Stites TE, Mitchell AE, Rucker RB. Physiological importance of quinoenzymes and the O-quinone family of cofactors. J Nutr. 2000 Apr;130(4):719-27.
- Choi O, Kim J, Kim JG, et al. Pyrroloquinoline quinone is a plant growth promotion factor produced by Pseudomonas fluorescens B16. Plant Physiol. 2008 Feb;146(2):657-68.
- Stites T, Storms D, Bauerly K, et al. Tchaparian. Pyrroloquinoline quinone modulates mitochondrial quantity and function in mice. J Nutr. 2006 Feb;136(2):390-6.
- Steinberg F, Stites TE, Anderson P, et al. Pyrroloquinoline quinone improves growth and reproductive performance in mice fed chemically defined diets. Exp Biol Med (Maywood). 2003 Feb;228(2):160-6.
- Bauerly KA, Storms DH, Harris CB, et al. Pyrroloquinoline quinone nutritional status alters lysine metabolism and modulates mitochondrial DNA content in the mouse and rat. Biochim Biophys Acta. 2006 Nov;1760(11):1741-8.
- Entrez Gene: PPARGC1A peroxisome proliferator-activated receptor gamma, coactivator 1 alpha [ Homo sapiens ] GeneID: 10891.
- Entrez Gene: CREBBP CREB binding protein [ Homo sapiens ] GeneID: 1387.
- Mitsumoto A, Nakagawa Y. DJ-1 is an indicator for endogenous reactive oxygen species elicited by endotoxin. Free Radic Res. 2001 Dec;35(6):885-93.
- Taira T, Saito Y, Niki T, Iguchi-Ariga SM, Takahashi K, Ariga H. DJ-1 has a role in antioxidative stress to prevent cell death. EMBO Rep. 2004 Feb;5(2):213-8.
- Paz MA, Martin P, Fluckiger R, Mah J, Gallop PM. The catalysis of redox cycling by pyrroloquinoline quinone (PQQ), PQQ derivatives, and isomers and the specificity of inhibitors. Anal Biochem. 1996 Jul 1;238(2):145-9.
- Urakami T, Yoshida C, Akaike T, Maeda H, Nishigori H, Niki E. Synthesis of monoesters of pyrroloquinoline quinone and imidazopyrroloquinoline, and radical scavenging activities using electron spin resonance in vitro and pharmacological activity in vivo. J Nutr Sci Vitaminol (Tokyo). 1997 Feb;43(1):19-33.
- Ohwada K, Takeda H, Yamazaki M, et al. Pyrroloquinoline quinone (PQQ) prevents cognitive deficit caused by oxidative stress in rats. J Clin Biochem Nutr. 2008 Jan;42:29-34.
- Nunome K, Miyazaki S, Nakano M, Iguchi-Ariga S, Ariga H. Pyrroloquinoline quinone prevents oxidative stress-induced neuronal death probably through changes in oxidative status of DJ-1. Biol Pharm Bull. 2008 Jul;31(7):1321-6.
- Ono K, Suzuki H, Sawada M. Delayed neural damage is induced by iNOS-expressing microglia in a brain injury model. Neurosci Lett. 2010 Apr 5;473(2):146-50.
- Zhang Y, Rosenberg PA. The essential nutrient pyrroloquinoline quinone may act as a neuroprotectant by suppressing peroxynitrite formation. Eur J Neurosci. 2002 Sep;16(6):1015-24.
- Hirakawa A, Shimizu K, Fukumitsu H, Furukawa S. Pyrroloquinoline quinone attenuates iNOS gene expression in the injured spinal cord. Biochem Biophys Res Commun. 2009 Jan 9;378(2):308-12.
- Jensen FE, Gardner GJ, Williams AP, Gallop PM, Aizenman E, Rosenberg PA. The putative essential nutrient pyrroloquinoline quinone is neuroprotective in a rodent model of hypoxic/ischemic brain injury. Neuroscience. 1994 Sep;62(2):399-406.
- Zhang Y, Feustel PJ, Kimelberg HK. Neuroprotection by pyrroloquinoline quinone (PQQ) in reversible middle cerebral artery occlusion in the adult rat. Brain Res. 2006 Jun 13;1094(1):200-6.
- Aizenman E, Hartnett KA, Zhong C, Gallop PM, Rosenberg PA. Interaction of the putative essential nutrient pyrroloquinoline quinone with the N-methyl-D-aspartate receptor redox modulatory site. J Neurosci. 1992 Jun;12(6):2362-9.
- Aizenman E, Jensen FE, Gallop PM, Rosenberg PA, Tang LH. Further evidence that pyrroloquinoline quinone interacts with the N-methyl-D-aspartate receptor redox site in rat cortical neurons in vitro. Neurosci Lett. 1994 Feb 28;168(1-2):189-92.
- Hossain MA. Molecular mediators of hypoxic-ischemic injury and implications for epilepsy in the developing brain. Epilepsy Behav. 2005 Sep;7(2):204-13.
- Dong XX, Wang Y, Qin ZH. Molecular mechanisms of excitotoxicity and their relevance to pathogenesis of neurodegenerative diseases. Acta Pharmacol Sin. 2009 Apr;30(4):379-87.
- Foran E, Trotti D. Glutamate transporters and the excitotoxic path to motor neuron degeneration in amyotrophic lateral sclerosis. Antioxid Redox Signal. 2009 Jul;11(7):1587-602.
- Hara H, Hiramatsu H, Adachi T. Pyrroloquinoline quinone is a potent neuroprotective nutrient against 6-hydroxydopamine-induced neurotoxicity. Neurochem Res. 2007 Mar;32(3):489-95.
- Zhang P, Xu Y, Sun J, Li X, Wang L, Jin L. Protection of pyrroloquinoline quinone against methylmercury-induced neurotoxicity via reducing oxidative stress. Free Radic Res. 2009 Mar;43(3):224-33.
- Kobayashi M, Kim J, Kobayashi N, et al. Pyrroloquinoline quinone (PQQ) prevents fibril formation of alpha-synuclein. Biochem Biophys Res Commun. 2006 Oct 27;349(3):1139-44.
- Zhang JJ, Zhang RF, Meng XK. Protective effect of pyrroloquinoline quinone against Abeta-induced neurotoxicity in human neuroblastoma SH-SY5Y cells. Neurosci Lett. 2009 Oct 30;464(3):165-9.
- Kim J, Kobayashi M, Fukuda M, et al. Pyrroloquinoline quinone inhibits the fibrillation of amyloid proteins. Prion. 2010 Jan;4(1):26-31.
- Takatsu H, Owada K, Abe K, Nakano M, Urano S. Effect of vitamin E on learning and memory deficit in aged rats. J Nutr Sci Vitaminol (Tokyo). 2009;55(5):389-93.
- Nakano M, Ubukata K, Yamamoto T, Yamaguchi H. Effect of pyrroloquinoline quinone (PQQ) on mental status of middle-aged and elderly persons. FOOD Style 21. 2009;13(7):50-3.
- Murase K, Hattori A, Kohno M, Hayashi K. Stimulation of nerve growth factor synthesis/secretion in mouse astroglial cells by coenzymes. Biochem Mol Biol Int. 1993 Jul;30(4):615-21.
- Zhu BQ, Zhou HZ, Teerlink JR, Karliner JS. Pyrroloquinoline quinone (PQQ) decreases myocardial infarct size and improves cardiac function in rat models of ischemia and ischemia/reperfusion. Cardiovasc Drugs Ther. 2004 Nov;18(6):421-31.
- Zhu BQ, Simonis U, Cecchini G, et al. Comparison of pyrroloquinoline quinone and/or metoprolol on myocardial infarct size and mitochondrial damage in a rat model of ischemia/reperfusion injury. J Cardiovasc Pharmacol Ther. 2006 Jun;11(2):119-28.
- Tao R, Karliner JS, Simonis U, et al. Pyrroloquinoline quinone preserves mitochondrial function and prevents oxidative injury in adult rat cardiac myocytes. Biochem Biophys Res Commun. 2007 Nov 16;363(2):257-62.
- Lang BF, Gray MW, Burger G. Mitochondrial genome evolution and the origin of eukaryotes. Annu Rev Genet. 1999;33:351-97.
- Bruce A, Johnson A, Lewis J, Raff M, Roberts K, Walter P. Molecular Biology of the Cell. New York, NY: Garland Publishing, Inc.;1994.
- Voet D, Voet JG, Pratt CW. Fundamentals of Biochemistry: Life at the Molecular Level. 2nd ed. New Jersey: John Wiley and Sons, Inc.; 2006:547.
- Pike RL, Brown M. Nutrition: An Integrated Approach. New York, NY: Prentice-Hall; 1984:450-84.
- Lanza IR, Nair KS. Mitochondrial function as a determinant of life span. Pflugers Arch. 2010 Jan;459(2):277-89.
- Robb EL, Page MM, Stuart JA. Mitochondria, cellular stress resistance, somatic cell depletion and lifespan. Curr Aging Sci. 2009 Mar;2(1):12-27.
- Alexeyev MF, LeDoux SP, Wilson GL. Mitochondrial DNA and aging. Clin Sci (Lond). 2004 Oct;107(4):355-64.
- Richter C. Oxidative damage to mitochondrial DNA and its relationship to ageing. Int J Biochem Cell Biol. 1995 Jul;27(7):647-53.
- Miquel J. An update on the mitochondrial-DNA mutation hypothesis of cell aging. Mutat Res.1992 Sep;275(3-6):209-16.
- Wallace DC. Mitochondrial DNA mutations in disease and aging. Environ Mol Mutagen. 2010 Jun;51(5):440-50.
- Wei YH, Lee HC. Oxidative stress, mitochondrial DNA mutation, and impairment of antioxidant enzymes in aging. Exp Biol Med (Maywood). 2002 Oct;227(9):671-82.
- Lee HC, Wei YH. Oxidative stress, mitochondrial DNA mutation, and apoptosis in aging. Exp Biol Med (Maywood). 2007 May;232(5):592-606.
- Wei YH, Ma YS, Lee HC, Lee CF, Lu CY. Mitochondrial theory of aging matures—roles of mtDNA mutation and oxidative stress in human aging. Zhonghua Yi Xue Za Zhi (Taipei). 2001 May;64(5):259-70.


